気液平衡とは?
密閉容器に液体を入れて放置すると、蒸発が起こります。しかし、ある一定時間放置すると、気体となった分子の一部が液体に戻り出し、見かけ上、蒸発が止まったような状態となります。これを気液平衡と呼びます。
液体分子も熱運動をしており、中には速度0m/sから高速に運動している分子も存在します(マクスウェル・ボルツマンの分布)。大きな熱運動を起こしている分子は、分子間の引力に逆らって、気体となることができます。一方、気体となった分子の一部は液体に衝突すると、分子間の引力に引き寄せられ、液体に戻ります。
このように、出る分子と入る分子の量が一定となっている状態を平衡と呼びます。
飽和蒸気圧(蒸気圧)とは?
気液平衡の状態となると、気体の分子の数は増加しません。この状態を飽和状態と呼びます。この飽和状態の気体が示す圧力を飽和蒸気圧(蒸気圧)と呼びます。蒸気圧は水銀圧力計で側生することができます。
蒸気圧の性質
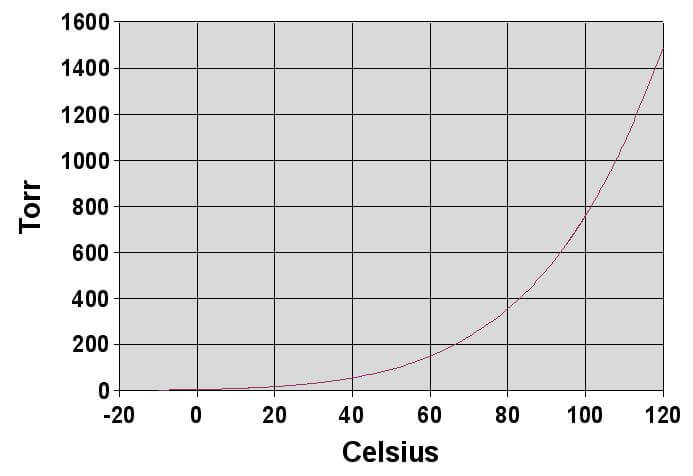
蒸気圧は、温度が一定ならば、それぞれの物質で決まった値を示します。また、液体の蒸気圧は、温度が上昇すると急激に大きくなります。この蒸気圧と温度の関係を示したグラフを蒸気圧曲線と呼びます。
温度の上昇と共に、蒸気圧が急激に上昇する理由は、温度が上がれば分子の熱運動は増すのに対し、分子間の引力は変化しないためです。熱運動が激しい分子の数は増えますが、気体から液体に戻る原子の数は僅かです。蒸気圧とは、気液平衡が成り立っている時の圧力のことを指します。そのため、気液平衡が成り立つためには、より多くの気体分子が存在する必要があり、その分蒸気圧も大きくなります。
蒸気圧には体積は関係ない
蒸気圧は、容器の体積がどのようなものであっても一定の値を示します。体積が大きくなればなるほど、蒸発が進むためです。
空間に他の気体があっても関係無い
また、空間に他の気体が存在してもしなくても、蒸気圧はほぼ一定の値を示します。これは、他の気体があったとしても、十分な空間があるためです。
しかし、厳密に言うと、圧力が高い空間においては、蒸気圧も徐々に上昇することが知られています。これは、液体分子が圧力によって押されることで反発し、気体となって飛び出していきやすくなるためです。
沸騰とは?
液体を加熱していくと、液体内部からも気泡が生じるようになります。この現象を沸騰と呼びます。沸騰は外圧(大気圧)と蒸気圧が等しくなることで起こります。そのため、気圧の低い場所では沸点が低くなり、気圧の高い場所では沸点は高くなります。
普通に考えれば、沸騰は水圧の影響を受けない液面で起こります。しかし、液面では、水圧が0ですが、液体の蒸発が盛んに起こっているため、温度が低い状態にあります。その結果、液面では沸騰は起こりません。しかし、底面では熱せられることよによって過熱状態となっており、水圧は高いですが、底面で気泡が発生します。
突沸はどうして起こるの?
沸騰は、容器の凸凹などに付着している気泡が、蒸気発生の起点となることが多いです。しかし、滑らかな容器を使っている場合には、中々沸騰が起こらないことがあります。この状態を過熱と言います。
過熱し続けていると、突如として大きな気泡が発生することがあります。この現象を突沸といいます。これを避けるためには、凸凹がある物質(沸騰石)を入れておきます。
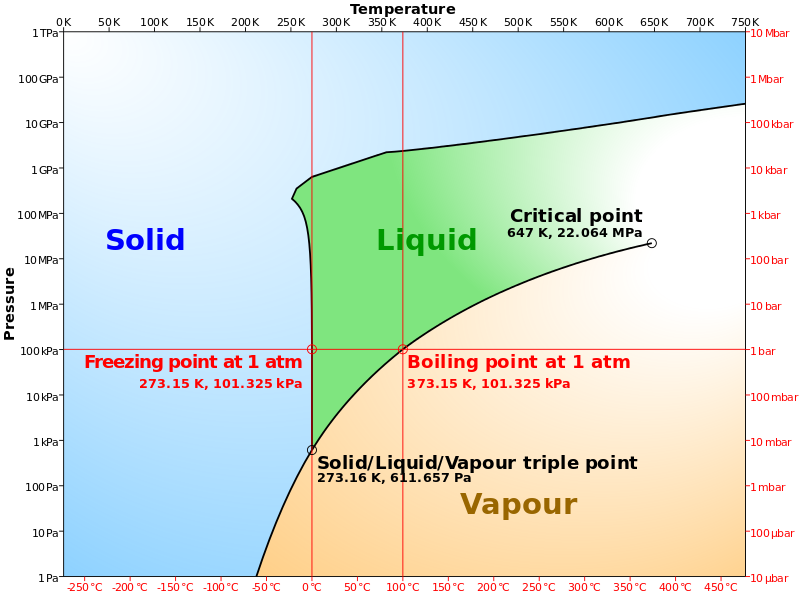
状態図とは?
ある温度・圧力で、物質が固体・液体・気体のどの状態であるかを示した図を状態図と呼びます。融点は圧力によって影響を殆ど受けないため、垂直に近いです。また、蒸気圧曲線は気体と液体が共存しているラインを示しているとも言えます。
また、氷を0℃の容器に入れて放置すると昇華が起こり、固体と気体が共存する状態となります。この固体と気体が共存している状態の圧力を示した曲線を昇華曲線と呼びます。
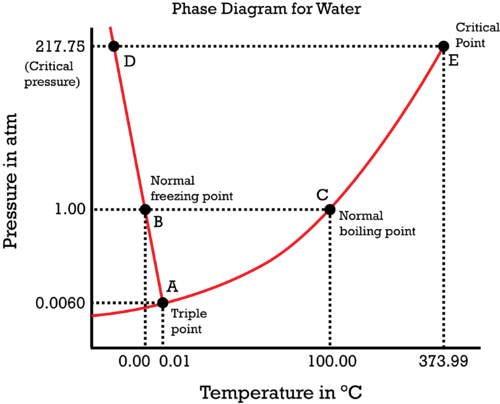
また、固体・液体・気体が平衡状態を保って存在しえる点を三重点と呼びます。水の三重点は温度の定点として利用されています。
水の融解曲線の傾きについて
水の融解曲線は左に傾いていますが、これは非常に珍しい物質です。つまり、加圧すると液体が増えるという物質です。これは、氷(固体)の密度よりも水(液体)の密度の方が高いために起こります。
https://courses.lumenlearning.com/
加圧すると液体に戻る性質は、スケートなどでも利用されます。スケートの刃で加圧された部分は液体になり、滑らかに滑ることができます。
また、下のような実験でも確かめることができます。
臨界点(臨界温度・臨界圧力)を超えるとどうなるの?
状態図には、臨界点が示されており、気体の状態でどんなに加圧しても液化しない点が存在します。これを臨界点と呼びます。下図ではcritical pointと書かれています。
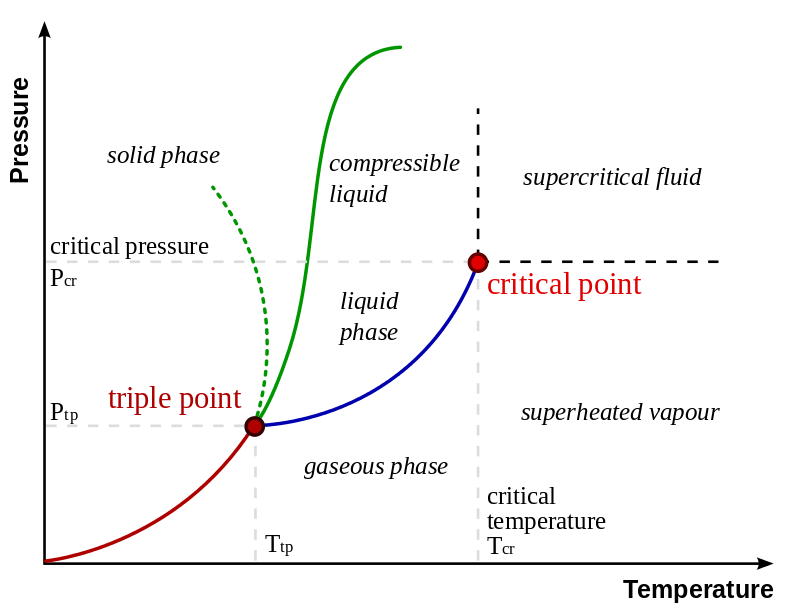
臨界点を突破すると、気体とも液体とも区別のつかない状態になります。つまり、液相と気相の界面がなくなり、すべて一相となります。この状態を超臨界流体と呼びます。液体と気体の両方の性質を合わせ持ちます。下動画は超臨界に達した二酸化炭素です。